Ένα μεγάλο βήμα προς την εύρεση τεχνικών για την «αναγέννηση» της καρδιάς μετά από έμφραγμα έκαναν επιστήμονες από το Τμήμα Βιοϊατρικής Μηχανικής του Πανεπιστημίου Duke, δίνοντας ελπίδες για λύση σε ένα δύσκολο πρόβλημα· o καρδιακός μυϊκός ιστός χάνει την ικανότητα να αναγεννάται μετά την πρώιμη παιδική ηλικία.
Σύμφωνα με τη μελέτη τους που δημοσιεύεται στο Science Advances, την επιτυχία στην αποκατάσταση του μυοκαρδίου, «του “ιερού δισκοπότηρου” της έρευνας για την καρδιά» όπως αναφέρεται στο δελτίο τύπου του Πανεπιστημίου, μπορεί πιθανότατα να εξασφαλίσει το ογκογονίδιο BRAF, που εμπλέκεται σε πολλούς τύπους καρκίνου, επί το πλείστον όμως σε δερματικούς όπως το μελάνωμα .
Το γονίδιο BRAF λειτουργεί ως οδηγός για την πρωτεΐνη B-Raf από το σηματοδοτικό μονοπάτι MARK, υπεύθυνο για σημαντικές κυτταρικές λειτουργίες που σχετίζονται με τη φυσιολογική ανάπτυξη (πολλαπλασιασμός, διαφοροποίηση, μετανάστευση, απόπτωση). Η μετάλλαξη στο γονίδιο οδηγεί σε υπερ-δραστηριότητα με αποτέλεσμα ανεξέλεγκτη ανάπτυξη και επιβίωση των κυττάρων.
Οι ερευνητές εισήγαγαν το ογκογονίδιο BRAF σε καρδιακό ιστό αρουραίων και είδαν ότι πράγματι άρχισε να προάγει την ανάπτυξη νέου ιστού. Εάν λοιπόν ένα τέτοιο γονίδιο μπορούσε να «τιθασευτεί» ώστε να χορηγηθεί με πλήρη έλεγχο της δραστηριότητάς του, θα μπορούσε να γίνει μια θεραπεία για την καρδιά εμφραγματιών.
«Τα ώριμα καρδιακά μυϊκά κύτταρα συνήθως δεν διαιρούνται, οπότε σκεφτήκαμε ότι θα χρειαζόμασταν μια ιδιαιτέρως ισχυρή γονιδιακή μετάλλαξη για να τα πείσουμε να πολλαπλασιαστούν» δήλωσε ο Nenad Bursac, καθηγητής Βιοϊατρικής Μηχανικής στο Duke. «Το MAPK είναι ένα καλά καταληπτό μονοπάτι που, όταν μεταλλάσσεται, μπορεί να γίνει αρκετά επιθετικό προκαλώντας υπερπολλαπλασιασμό σε κακοήθειες, γι’ αυτό και επιλέξαμε να το εξετάσουμε».
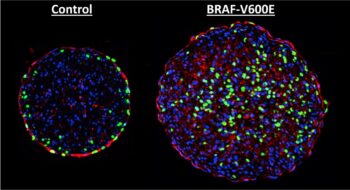
Δύο δείγματα τεχνητού καρδιακού ιστού αρουραίου που δείχνουν τη μετάλλαξη BRAF εν δράσει. Το τροποποιημένο κύτταρο BRAF στα δεξιά έχει περισσότερο νεοσυντιθέμενο DNA (πράσινο χρώμα), γεγονός που δείχνει ότι η μετάλλαξη προκαλεί κυτταρική διαίρεση. (Πηγή: Duke Pratt School of Engineering)
Ενεργοποιώντας τη μετάλλαξη
Ο Δρ Bursac και ο διδακτορικός φοιτητής Nicholas Strash μελέτησαν καρδιακά κύτταρα νεογέννητων αρουραίων που αναπτύχθηκαν μέσα σε υδρογέλη και παρείχαν ενδείξεις για την ανάπτυξη και την ωρίμανση των κυττάρων σε ενήλικους καρδιακούς μυϊκούς ιστούς, όπου η κυτταρική διαίρεση σταματά φυσιολογικά.
Οι υδρογέλες, όπως αυτή που ανέπτυσσαν πάνω από μια δεκαετία οι ερευνητές, αποτελούν υδρόφιλα πολυμερικά δίκτυα με τρισδιάστατη διαμόρφωση που αναδεικνύονται οι πλέον υποσχόμενες για κυτταρικές καλλιέργειες λόγω των ειδικών δομών και ιδιοτήτων τους, όπως η μίμηση των σημαντικότερων χαρακτηριστικών της εξωκυττάριας μήτρας.
Οι ερευνητές μόλυναν τα καρδιακά μυϊκά κύτταρα με ιό που έφερε τη μετάλλαξη BRAF, η οποία έδρασε κατά τον συνήθη τρόπο: το μεταλλαγμένο γονίδιο εισήλθε στα κύτταρα και ενσωματώθηκε στο DNA τους. Στη συνέχεια, οι ερευνητές ενεργοποίησαν τα μεταλλαγμένα γονίδια με χορήγηση ενός φαρμάκου.
Όπως με τον καρκίνο του δέρματος, τα ενεργοποιημένα ογκογονίδια ώθησαν τα καρδιακά μυϊκά κύτταρα σε σύνθεση DNA, το πρώτο βήμα της κυτταρικής διαίρεσης και ανάπτυξης.
Εμπόδια και αδυναμίες
Σύμφωνα με τους ερευνητές, υπάρχουν ζητήματα που χρήζουν διερεύνησης αναφορικά με τη δοσολογία και τη διάρκεια της γονιδιακής ενεργοποίησης.
Θα πρέπει αρχικά να βρεθεί διαφορετικό σύστημα χορήγησης ώστε τα γονίδια να μεταφερθούν στα σωστά κύτταρα με τρόπο που θα επιτρέπει τον πλήρη έλεγχό τους . Μέθοδοι όπως τα λιπιδικά νανοσωματίδια και οι βραχύβιοι ιοί είναι δύο προσεγγίσεις που, αν και υπό ανάπτυξη επί του παρόντος, απέχουν από τη δυνατότητα εφαρμογής τους για την αναγέννηση της καρδιάς στον άνθρωπο.
Έπειτα, θα πρέπει να βρεθεί λύση για ένα σημαντικό μειονέκτημα: τα κύτταρα, στη φάση του πολλαπλασιασμού τους, άρχισαν να αποσυναρμολογούν τους μηχανισμούς που ευθύνονται για τη συστολή και την άντληση του αίματος, με αποτέλεσμα τη μείωση της συσταλτικής δύναμης κατά 70%.
Με βάση το χρονοδιάγραμμα των κυτταρικών μηχανισμών, η ομάδα πιστεύει ότι μπορεί να υπάρχει ένα χρονικό παράθυρο στο οποίο η δραστηριότητα του μεταλλαγμένου γονιδίου θα μπορούσε να διακοπεί, μετά την έναρξη της αντιγραφής και πριν επηρεαστεί ο μηχανισμός συστολής σε μεγάλο τμήμα του μυοκαρδίου. Ένα άλλο σενάριο θα ήταν η εφαρμογή μιας δεύτερης παρέμβασης που θα μπορούσε να ωθήσει τα κύτταρα να ξαναχτίσουν τον αποσυναρμολογημένο μηχανισμό άντλησης μετά τον πολλαπλασιασμό.
Η επόμενη ημέρα
Οι ερευνητές σχεδιάζουν να μελετήσουν τη λειτουργία της παρέμβασης στις καρδιές πειραματόζωων και να τη συγκρίνουν με τα εργαστηριακά τους αποτελέσματα. Έτσι, θα κατανοήσουν καλύτερα και ποια ακόμα γονίδια και διαδικασίες ενεργοποιούνται από τη μετάλλαξη BRAF.
Διαβάστε επίσης:
Καρδιά – Έμφραγμα: Αυτοί οι μεσήλικες κινδυνεύουν περισσότερο
Στεφανιαία νόσος: Όλα όσα (πρέπει να) αλλάζουν στη ζωή μετά το έμφραγμα
Η απλή άσκηση που μπορεί να προλάβει καρδιαγγειακές νόσους και διαβήτη







