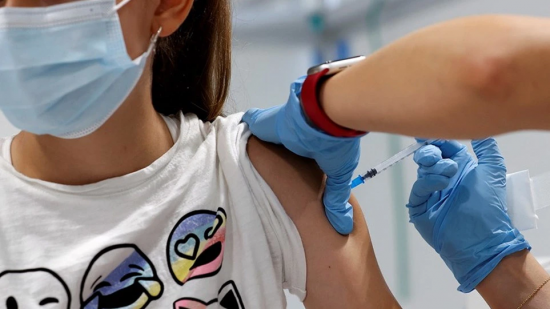
Τα δεδομένα από τις δοκιμές Φάσης 2/3 του εμβολίου τους κατά της Covid-19 σε παιδιά ηλικίας από 5 ως 12 ετών, υπέβαλλαν οι Pfizer και BioNTech στον Οργανισμό Τροφίμων και Φαρμάκων των ΗΠΑ (FDA), στο πλαίσιο της ανασκόπησης για την έγκριση επείγουσας χρήσης του εμβολίου.
Στη δοκιμή, η οποία περιελάμβανε 2.268 συμμετέχοντες ηλικίας 5 έως 12 ετών, το εμβόλιο έδειξε καλά δεδομένα ασφάλειας και προκάλεσε ισχυρά εξουδετερωτικά αντισώματα, με τη χρησιμοποίηση ενός σχήματος δύο δόσεων των 10 mg.
It’s official: We have submitted initial data from the pivotal trial of our COVID-19 vaccine in children 5 to under 12 years of age to the @US_FDA: https://t.co/XORlEFksAs
— AlbertBourla (@AlbertBourla) September 28, 2021
Αυτά τα αποτελέσματα -τα πρώτα από μια δοκιμή οποιουδήποτε εμβολίου κατά της Covid-19 σε αυτήν την ηλικιακή ομάδα – ήταν συγκρίσιμα με τα καταγεγραμμένα σε προηγούμενη μελέτη των Pfizer-BioNTech σε άτομα ηλικίας 16 έως 25 ετών, τα οποία ανοσοποιήθηκαν με δόσεις των 30 mg.
Τις επόμενες εβδομάδες αναμένεται να ακολουθήσει επίσημη υποβολή στον FDA με την αίτηση Εξουσιοδότησης Επείγουσας Χρήσης (EUA) σε παιδιά αυτών των ηλικιών. Προβλέπονται, επίσης, ανάλογες υποβολές στον Ευρωπαϊκό Οργανισμό Φαρμάκων (ΕΜΑ) και σε άλλες ρυθμιστικές αρχές.
Δεδομένα για τις δοκιμές του εμβολίου στις άλλες δύο ηλικιακές ομάδες – παιδιά 2 έως 5 ετών και παιδιά 6 μηνών έως 2 ετών – αναμένονται μέσα στο τέταρτο τρίμηνο του τρέχοντος έτους.